2025. 4. 18. 11:33ㆍ[2022개정_통합과학]

오늘은 우리가 과학 시간에 자주 보는
‘주기율표’, 이걸 어떻게 읽는지
그리고 어떤 기준으로 만들어졌는지
처음부터 쫙 정리해볼게.
먼저, 주기율표는 어떻게 발전해왔을까?
처음엔 되베라이너라는 과학자가
성질이 비슷한 원소 3개씩 묶으면
가운데 원자량이 양쪽 평균쯤 되더라~ 하고
세쌍 원소설을 제안했어.
그다음엔 뉴랜즈라는 과학자가
**8번째마다 성질이 비슷해진다!**는 걸 발견하고
옥타브설이라고 불렀지. (도레미파솔라시도~ 처럼)
그리고 나서 멘델레예프가
원자량 순으로 정리한 주기율표를 만들었고
미발견 원소까지 예측했어. 진짜 대단했지.
근데!
원자량만으로 정리하다 보니까
성질이 안 맞는 부분이 생겨서,
그걸 모즐리라는 과학자가 정리했어.
→ “원자번호 순서대로 정리해야 성질이 딱딱 맞는다!”
이렇게 해서 지금 우리가 사용하는 주기율표는
‘원자번호 기준’으로 배열된 거야.
주기율표 구조 알아보자
주기율표는
가로줄은 ‘주기’,
세로줄은 ‘족’이라고 해.
- 1주기, 2주기, 3주기… 7주기까지
- 1족부터 18족까지 있어
✔ 같은 주기에 있는 원소들은
→ 전자 껍질 수가 같고
✔ 같은 족에 있는 원소들은
→ 원자가 전자 수가 같아서 성질이 비슷해
예를 들어
- 1족 원소는 전자가 1개,
- 2족은 2개,
- 13족은 3개…
- 17족은 7개,
- 18족은 예외로 0개 (거의 반응 안 함)
금속이냐 비금속이냐?
주기율표에서
- 왼쪽은 대부분 금속 원소,
- 오른쪽은 대부분 비금속 원소야.
근데 예외가 하나 있어.
→ 수소!
위치는 왼쪽 1족에 있지만
성질은 비금속이야.
그리고 금속과 비금속의 경계선 근처엔
둘 다 섞인 듯한 중간 성질을 가진 원소들도 있어.
금속 vs 비금속 차이
- 금속 원소:
→ 양이온 되기 쉬움, 대부분 고체
→ 예외: 수은(Hg)은 액체야 - 비금속 원소:
→ 음이온 되기 쉬움, 대부분 고체나 기체
→ 예외: 브로민(Br)은 액체 상태야
족별로 꼭 알아둬야 할 대표 원소들!
1족 (알칼리 금속)
- 수소 제외! 나머지는 전자를 1개 잃고 1가 양이온
- 금속 중 반응성이 가장 큼
17족 (할로젠 원소)
- 전자 1개 받아서 1가 음이온
- 대부분 이원자 분자로 존재
- 비금속 중 반응성이 제일 강함
18족 (비활성 기체)
- 전자가 꽉 차 있음 → 반응 거의 안 함
- 전부 일원자 분자로 존재
- 헬륨, 네온, 아르곤 같은 애들
자, 단순화된 주기율표로 정리해보자
단순화된 주기율표는
딱 핵심 원소들만 간단히 외우기 쉽게 구성된 거야.
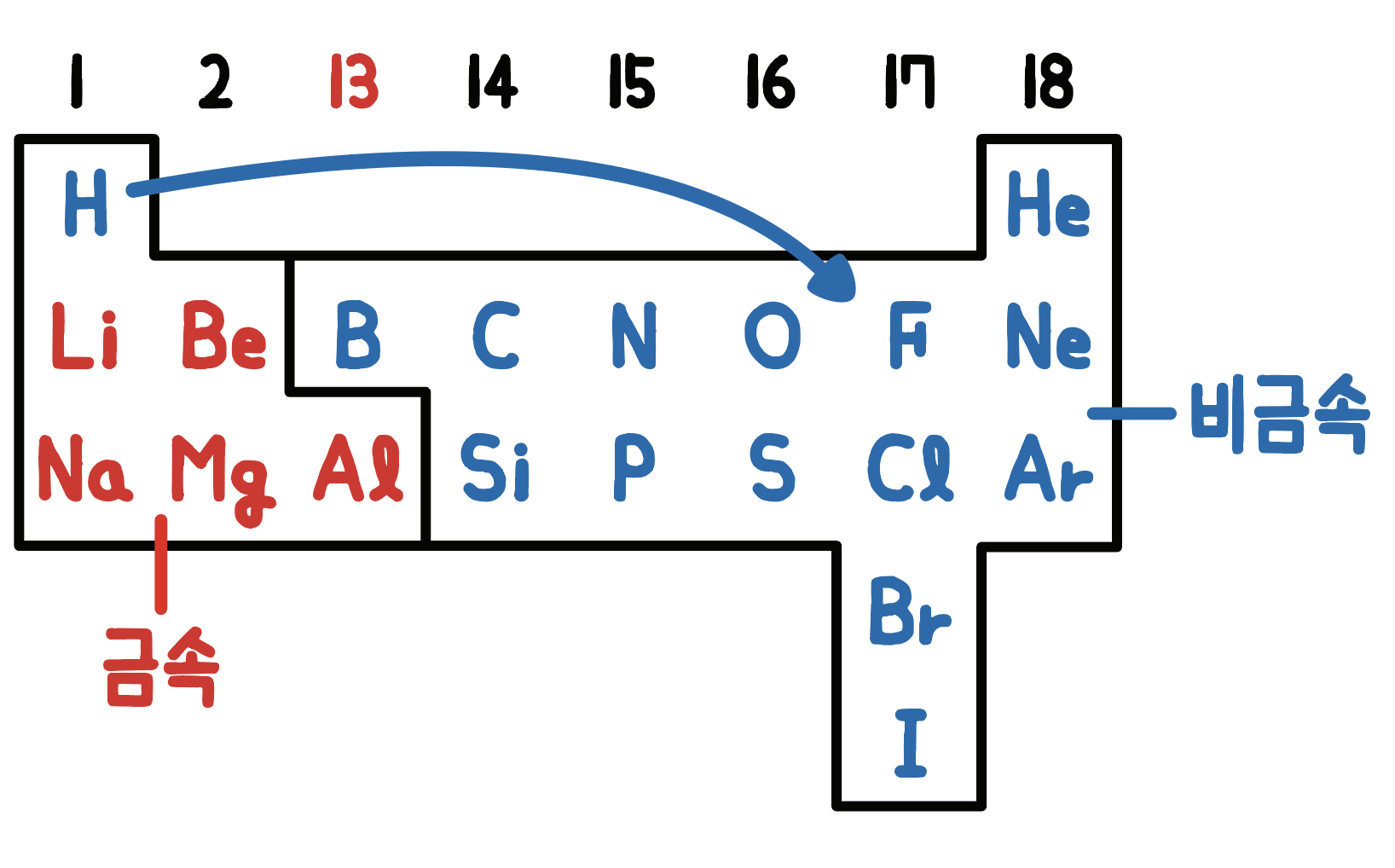
이 주기율표만 정확하게 외워도 족, 주기, 금속/비금속, 반응성 다 잡을 수 있어.
이제 주기율표는 단순히 외우는 게 아니라
어떻게 정리됐고,
원소들 성질이 어떻게 연결되는지까지 이해해야
과학이 훨씬 쉬워지고 재밌어져.
'[2022개정_통합과학]' 카테고리의 다른 글
| [통합과학] 알칼리 금속과 할로젠 원소 (0) | 2025.04.20 |
|---|---|
| [통합과학] 원자의 전지 배치 (0) | 2025.04.20 |
| [통합과학] 원시 지구 진화 (0) | 2025.04.15 |
| [통합과학] 태양계 형성과 행성(지구형/목성형) (0) | 2025.04.15 |
| [통합과학] 변의 탄생과 진화 (0) | 2025.04.09 |