2021. 11. 2. 18:52ㆍ[중등2] 6단원 : 물질의 특성
자. 이번 수업은 용해도와 석출량에 대해 알아보자.
용해도는 어떤 물질이 용매, 즉 물 100g에 최대한 녹을 수 있는 용질의 g수를 말한다.
예를 들어 어떤 물질의 물에 대한 용해도가 60이라면
물 100g에는 이 물질이 최대 60g이 녹을 수 있다는 것이고
물 50g에는 최대 30g이 녹을 수 있으며
물 200g에는 최대 120g이 녹을 수 있다는 의미이다.
석출은 용질이 녹아 있는 용액을 냉각시킬 때 녹아 있던 용질이
고체 상태로 용액에서 분리되는 현상을 말한다.
이 때 석출되는 용질의 양은 처음 용액에 녹아 있던 용질의 양에서
냉각한 온도에서 최대한 녹을 수 있는 용질의 양을 빼는 것으로 구할수 있다.
예를 들어 질산나트륨의 용해도 곡선이 다음과 같고
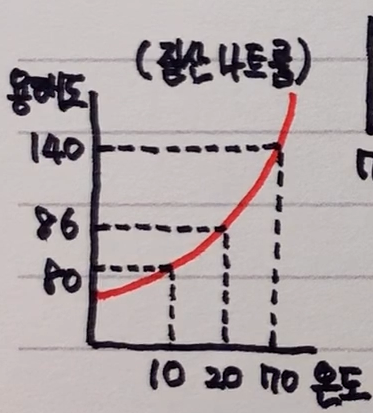
70도씨 물 100g에 질산나트륨을 120g 녹인 후 10도씨로 냉각 시켰을 때 석출량을 구해보자.
10도씨에서 질산나트륨의 용해도는 80이고
이것은 물 100g에 최대한 녹을 수 있는 질산나트륨, 즉 용질의 양은 80g이라는 뜻이므로
120g 중 80g은 물에 녹아 있지만
나머지 40g은 녹지 못하고 고체 상태로 석출된다.
따라서 석출량은 처음 녹아 있던 용질 120에서
냉각한 온도에서 최대한 녹을 수 있는 용질 양 80을 빼는 것으로 계산할 수 있다.

두 개의 예제를 통해 석출량 구하는 방법에 대해 조금 더 알아보자.
첫번째 예제는
70도씨 물 50g에 질산나트륨 60g을 녹인 후 다시 20도씨로 냉각시켰을 때 석출량이 얼마인지를 묻는 문제이다.

20도씨에서 질산나트륨의 용해도는 86이고
물 50g에 녹을 수 있는 질산나트륨의 양은 용해도의 절반인 43g이다.
따라서 석출량은
처음 용질의 양 60에서 녹을수 있는 용질 양 43을 뺀 17g이 된다.
두 번째 예제는
70도씨 물 200g에 질산나트륨을 240g 녹인 후 20도씨로 냉각했을 때의 석출량을 묻는 문제이다.

20도씨에서 질산나트륨의 용해도는 86이고
물이 200g이므로, 녹을수 있는 용질의 양은 용해도의 두배인 172g이 된다.
따라서 석출량은 처음 용질의 양 240에서 녹을 수 있는 용질의 양 172를 뺀 68g이 된다.
탑사이언스 과학학원(대구 수성구)
www.topsa.co.kr
'[중등2] 6단원 : 물질의 특성' 카테고리의 다른 글
| [중등2과학] 기체의 용해도 (0) | 2021.11.04 |
|---|---|
| [중등2과학] 포화수용액과 석출량 (0) | 2021.11.02 |
| [중등2과학] 밀도 (0) | 2021.10.31 |
| [중등2과학] 끓는점, 녹는점, 어는점 (0) | 2021.10.31 |
| [중등2과학] 물질의 분류와 물질의 특성 (0) | 2021.10.31 |